碳酸鍶編號系統
CAS號:1633-05-2
MDL號:MFCD00011250
EINECS號:216-643-7
PubChem號:24852270
碳酸鍶造價信息
WGK Germany -
毒害物質數據 1633-05-2(Hazardous Substances Data)
| 中文名稱 |
碳酸鍶 |
| 英文名稱 |
Strontium carbonate,nanometre |
| 中文別名 |
碳酸鍶(納米); 粒品碳酸鍶 ; 菱鍶礦 ; 碳酸鍶(1:1) ; 碳酸鍶 ; 高純碳酸鍶; 碳酸鍶(電子級) |
| 英文別名 |
C.I. 77837; Strontium carbonate; Strontium carbonate,high purity; Strontium carbonate,electronic grade; Strontiumcarbonate |
| CAS號 |
1633-05-2;1633-55-2 |
| EINECS號 |
216-643-7 |
| 分子式 |
SrCO3 |
| 分子量 |
147.63 |
| InChI |
InChI=1/CH2O3.Sr/c2-1(3)4;/h(H2,2,3,4);/q; 2/p-2 |
| 熔點 |
1497℃ |
| 密度 |
3.7 |
| 用途 |
用于生產納米材料、電子元件、焰火材料、彩虹玻璃、其他鍶鹽制備、PTC熱敏電阻元件(開關啟動、消磁、限流保護、恒溫發熱等)生產的基礎粉料 |
相關類別: Inorganic Chemicals;Inorganics;Chemical Synthesis;Inorganic BasesMetal and Ceramic Science;Salts;Strontium Salts;Synthetic Reagents;Cd硝酸鹽;無機化工產品;無機鹽;metal carbonate;輕金屬;Chemical Synthesis;Inorganic Bases;Materials Science;Metal and Ceramic Science;Strontium Salts;Synthetic Reagents;無機鍶鹽;催化和無機化學;通用試劑;鍶;有機化工
Mol文件: 1633-05-2.mol
碳酸鍶編號系統常見問題
-
此外,橡膠用超細碳酸鈣其吸收油值越高,碳酸鈣對橡膠的浸潤性和補強性越好,通過應用發現,在不同晶形的超細鈣中,以鏈鎖狀超細碳酸鈣對橡膠的補強效果最好。塑料工業是我國超細碳酸鈣行業最大的用戶之一,也是應用...
-
重質碳酸鈣鈣粒度是400~2500目之間的高白度精細粉末,是選用優質方解石礦石,它具有含量純度高,白度高、粒徑均勻,同時還具有無臭、無味、無腐蝕、無放射、符合環保條件等特點。由于重鈣本身具有良好的分散...
-
我專門研究銫銣。碳酸銫和碳酸鉀有相似性,也有不同點。看你做什么了。主要是看你做什么了。碳酸銫和碳酸鉀是化學上說的所謂鹽,但是水溶液顯堿性!
性狀:無色斜方晶系或白色細微粉末。無臭。無味
密度(g/mL,25/4℃): 3.7
相對蒸汽密度(g/mL,空氣=1):未確定
熔點(oC):1497(CO2氣氛下)
沸點(oC,常壓):2647
沸點(oC,5.2kPa): 未確定
折射率: 未確定
閃點(oC): 未確定
比旋光度(o): 未確定
自燃點或引燃溫度(oC): 未確定
蒸氣壓(kPa,25oC): 未確定
飽和蒸氣壓(kPa,60oC): 未確定
燃燒熱(KJ/mol):未確定
臨界溫度(oC): 未確定
臨界壓力(KPa): 未確定
油水(辛醇/水)分配系數的對數值: 未確定
爆炸上限(%,V/V):未確定
爆炸下限(%,V/V): 未確定
溶解性:易溶于氯化銨、硝酸銨溶液,難溶于水,微溶于氨水、碳酸銨和CO2飽和水溶液,不溶于醇,
吸入鍶化合物粉塵,能引起兩肺中度彌漫性間質改變。最高容許濃度為6mg/m3。
通常對水是不危害的,若無政府許可,勿將材料排入周圍環境。
疏水參數計算參考值(XlogP):無
氫鍵供體數量:0
氫鍵受體數量:3
可旋轉化學鍵數量:0
互變異構體數量:無
拓撲分子極性表面積63.2
重原子數量:5
表面電荷:0
復雜度:18.8
同位素原子數量:0
確定原子立構中心數量:0
不確定原子立構中心數量:0
確定化學鍵立構中心數量:0
不確定化學鍵立構中心數量:0
共價鍵單元數量:2
菱鍶礦是一種碳酸鹽礦物。 菱鍶礦化學組成SrO 70.19%、CO2 29.81%,常含錳、鋇和鈣。硬度3.5,性脆,相對密度3.76。通常為白色,有時因含雜質,而成灰、黃、白、淺綠或褐色等,條痕白色。斜方晶系完全菱面體解理,玻璃光澤,斷面呈油脂光澤,貝殼狀斷口。溶于稀鹽酸,產生氣泡。與方鉛礦、閃鋅礦和黃銅礦伴生于含硫化物的礦脈中,也與方解石、白云石以及石英伴生。
下游產品 氯化鍶-->硝酸鍶-->2,6-二甲基辛醛-->鉻酸鍶鈣-->氫氧化鍶-->氫氧化鍶八水合物-->氧化鍶-->氟化鍶
上游原料 碳酸鈉-->硫酸鈉-->二氧化碳-->碳酸氫銨-->碳酸銨-->焦炭(煤)-->十水合硫酸鈉-->氯化鍶-->礦粉-->硝酸鍶-->硫酸鍶
第一種復分解法
將天青石粉碎后與純堿溶液反應2h,反應溫度100℃。碳酸鈉起始濃度20%,碳酸鈉加入量為理論量的110%,礦粉粒度80目,在此條件下,分解率可達97%以上,經過濾,濾液中硫酸鈉濃度可達24%。粗制碳酸鍶用水打漿,加鹽酸調料漿至pH3,在溫度90~100℃下經2~3h,加入除鋇劑除鋇,再用氨水調漿液至pH6.8~7.2除雜,過濾后濾液用碳酸氫銨或碳酸銨溶液沉淀出碳酸鍶,再過濾除去氯化銨溶液,濾餅經干燥,制得碳酸鍶成品。其
SrSO4 Na2CO3→SrCO3 Na2SO4
SrCO3 2HCl→SrCl2 CO2↑ H2O
SrCl2 NH4HCO3→SrCO3 NH4Cl HC
第二種煤還原法
天青石和煤粉經粉碎,以通過20目的作為原料,礦煤比為1:0.6~1:0.7,在溫度1100~1200℃下還原焙燒,經0.5~1.0 h,焙燒物經兩次浸取,一次水洗,浸取溫度90℃,每次浸3h,總浸出率可達82%以上,浸液經過濾,濾渣經鹽酸溶浸后進一步回收鍶,濾液中加芒硝溶液除鋇,再加入碳酸氫銨或碳酸鈉溶液進行反應生成碳酸鍶沉淀(或直接用二氧化碳碳化),再經分離、干燥、球磨粉碎,制得碳酸鍶成品。其
SrSO4 2C→SrS 2CO2
2SrS十2H2O→Sr(OH)2 Sr(HS)2
Sr(OH)2 Sr(HS)2 2NH4HCO3→2SrCO3 2NH4HS 2H2O
第三種菱鍶礦熱解法
將菱鍶礦和焦炭粉碎,按礦:焦=10:1(重量比)的比例配成混合料,經1150~1250℃溫度下焙燒,使碳酸鹽分解生成含氧化鍶和其他金屬氧化物熟料。熟料經三級浸取,浸取溫度以95℃為佳,二、三級浸取可在。70-80℃下進行。浸取液使氫氧化鍶濃度為:1mol/L,有利于雜質Ca2 、Mg2 的分離,向濾液加入碳酸氫銨進行碳化而得碳酸鍶,再經分離、烘干、粉碎,制得碳酸鍶成品。其
SrCO3→SrO CO2↑
SrO H2O→Sr(OH)2
Sr(OH)2 NH4HCO3→SrCO3↓ NH3·H2O H2O
第四種綜合利用法 從含溴、鍶的地下鹵水中,經提溴后的含鍶母液用石灰中和,經蒸發濃縮、冷卻,除去氯化鈉,再經燒堿除鈣,加碳酸氫銨使氫氧化鍶轉化成碳酸鍶沉淀,再經漂洗、烘干,制得碳酸鍶成品。其
SrCl2 2NaOH→Sr(OH)2 2NaCl
Sr(OH)2 NH4HCO3→SrCO3 NH3·H2O H2O
用于制造彩電陰極射線管、電磁鐵、鍶鐵氧體、煙火、熒光玻璃、信號彈等,也是生產其他鍶鹽的原料;用作專用PTC熱敏電阻元件(開關啟動、消磁、限流保護、恒溫發熱等)生產的基礎粉料。
作為鈀的載體,可作加氫之用。此外,還用于造紙、醫藥、分析試劑,以及糖的精制、金屬鋅電解液精制、鍶鹽顏料制造等。
質檢信息質檢項目指標值
| 質檢項目 |
項目指標值 |
|---|---|
| 澄清度試驗 |
合格 |
| 含量(SrCO3) |
≥99.0 |
| 鹽酸不溶物 |
≤0.007 |
| 重金屬(以Pb計) |
≤0.002 |
| 鐵(Fe) |
≤0.001 |
| 鋇(Ba) |
≤0.05 |
| 鈣及鎂(以Ca計) |
≤0.05 |
| 氯化物(Cl) |
≤0.001 |
| 硫酸鹽(SO4) |
≤0.01 |
| 硝酸鹽(NO3) |
≤0.015 |
一種以天青石為原料,經預處理,使用轉化劑轉化反應,凈化處理、純碳酸鍶產品制取等四道工序生產碳酸鍶的工藝方法,本發明的特征是:
預處理是采取加入除鈣劑并控制溫度于60~90℃反應0.5~2小時的工藝,其中除鈣劑的加入量為理論量的125~175%,可采用濃鹽酸或濃硝酸或濃硫酸作除鈣劑,
轉化反應是采用碳酸氫銨作轉化劑,將預處理過的天青石在氫氧化銨的存在下與固體碳酸氫銨相混合,于65~80℃反應3.5~7小時的工藝,其中氫氧化銨的用量為天青石量的120~180%,碳酸氫銨的用量為天青石量的130~170%,
凈化處理是加入8~12N的鹽酸,控制溫度于60~90℃溶解反應,反應完全后加入除鋇劑,隨后再加入氫氧化銨至PH=6~8的工藝,其中鹽酸的用量控制在理論量的103~110%,除鋇劑用量控制在理論量的20~50%,除鋇劑可采用鉻酸鉀或鉻酸鈉或重鉻酸鉀或重鉻酸鈉或硫酸銨,
純碳酸鍶產品制取是將氯化鍶凈化液控制加熱至50~80℃,在氫氧化銨存在下加入碳酸氫銨飽和溶液進行反應的工藝,其中氫氧化銨的用量控制在理論量的102~120%,碳酸氫銨飽和溶液的加入量控制在理論量的102~120%。
碳酸鍶編號系統文獻

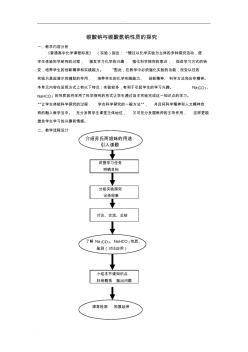 碳酸鈉與碳酸氫鈉性質的探究教學設計
碳酸鈉與碳酸氫鈉性質的探究教學設計
格式:pdf
大小:229KB
頁數: 9頁
評分: 4.6
. . 碳酸鈉與碳酸氫鈉性質的探究 一、教學內容分析 《普通高中化學課程標準》 (實驗)指出: “通過以化學實驗為主體的多種探究活動,使 學生體驗科學研究的過程, 激發學習化學的興趣, 強化科學探究的意識, 促進學習方式的轉 變,培養學生的創新精神和實踐能力。 ”因此,在教學中必須強化實驗的功能,改變以往的 實驗只是起演示和輔助的作用, 培養學生的化學實踐能力、 創新精神、 科學方法和合作精神。 本單元內容在呈現方式上有以下特點:實驗較多,有利于引起學生的學習興趣。 Na2CO3、 NaHCO 3 的性質我將采用了科學探究的形式讓學生通過自主實驗完成這一知識點的學習。 “讓學生體驗科學探究的過程, 學會科學探究的一般方法”, 并且將科學精神和人文精神自 然的融入教學當中。 充分發揮學生課堂主體地位, 又可充分發掘教師的主導作用, 這樣更能 激發學生學習的興趣和情感。 二、教學流程設計
兩次世界大戰期間,鍶化合物廣泛用于生產煙火及信號彈;本世紀二三十年代,用碳酸鍶作煉鋼的脫硫劑,以除去硫、磷等有害雜質;50年代,在電解鋅生產中,用碳酸鍶提純鋅,其純度可達99.99%;60年代末,碳酸鍶廣泛用作磁性材料;鈦酸鍶用于電子計算機存儲器,氯化鍶用作火箭燃料;1968年發現碳酸鍶屏蔽X射線的功能,并將其應用于彩色電視機熒屏玻璃,現需求量正在大幅度增長;鍶在其他領域中也不斷地擴大其應用范圍。從此,鍶碳酸鹽和其他鍶化合物(鍶鹽)作為重要的無機鹽原料,受到人們普遍的關注與重視。 根據世界對鍶需求的穩步增長及中國豐富的鍶礦資源和良好的鍶礦找礦前景,鍶礦資源除滿足中國國民經濟發展過程中自身需求外,還可發展鍶礦資源及其多種制品外向型礦業經濟,參與國際競爭。因此,鍶礦資源不但是世界上重要的戰略性礦產資源,而且在中國國民經濟中的地位與作用,也將日益上升、日趨重要。

碳酸鍶礦共生產物
硫酸鍶(SrSO4)
比重3.96,溶點1580℃,為白色粉末,溶于熱濃硫酸,微溶于水、稀鹽酸和稀 硝酸。硫酸鍶是天青石礦物的主要化學成分,是生產碳酸鍶的原料,主要用于煙火、陶瓷工業和作燒堿的脫鐵劑。 碳酸鍶(SrCO3)
比重3.7,熔點1497℃。碳酸鍶是目前運用最廣的鍶化合物,用它制造的玻璃能吸收X射線,是生產彩色電視陰極射線管和熒光屏的原料,但碳酸鍶的純度要求高(Sr/BaCO3>98%)。在冶金工業中可作制取高純鋅精煉的脫鉛劑。
硝酸鍶Sr(NO3)2
比重2.986,熔點570℃。硝酸鍶是氧化劑,與有機物接觸、摩擦、碰撞、遇火能引起燃燒和爆炸,發出深色火焰。因此硝酸鍶主要用于制造紅色煙火和各種信號彈、火焰筒、火柴。
鉻酸鍶(SrCrO4)
比重3.9。向油漆中加入鉻酸鍶,可形成一層防腐層,該防護層可以有效地保護鋁,尤其是飛機機殼和船體。因此鉻酸鍶主要用于制造防銹顏料。
鐵酸鍶(SrFe12O18)
具有較高的矯頑力、良好的熱阻性、電阻性及化學穩定性,能夠抵抗脫磁,因此鐵酸鍶可生產永久陶瓷磁鐵,廣泛運用于直流電機、揚聲器及電磁鐵的生產中。
碳酸鍶礦
鈦酸鍶(SrTiO3)
鈦酸鍶是一種高技術的鍶陶瓷,在有些半導體中用作基片,在光學和壓電學方面用作感光片,亦用于生產電子計算機存儲器。 氧化鍶(SrO)
比重4.5,熔點2430℃,用于煙火、顏料、 醫藥等方面。
硫化鍶(SrS)
可用在某些發光性和磷光性顏料中作活性配料。
氯化鍶(SrCl2·6H2O)
可用于煙火、火箭燃料及醫藥工業。
氫氧化鍶〔Sr(OH)2〕和鍶水化合物〔Sr(OH)2·8H2O〕
可用于生產鍶潤滑膏和肥皂,前者又可用作吸附劑及塑料膠。

碳酸鍶礦基本資料
碳酸鍶礦(菱鍶礦)(Strontianite) Sr[CO3]
晶體化學
理論組成(wB%):SrO 70.19,CO2 29.81。常有Ca置換Sr,一般天然碳酸鍶礦的Ca:Sr<1:4.5;有時Ca含量可達10.6%。SrCO3-BaCO3之間可形成完全類質同像。但天然碳酸鍶礦的Ba含量很少,只達2~3%。變種有鈣碳酸鍶礦、鋇碳酸鍶礦。
結構與形態
斜方晶系,a0=0.5128nm,b0=0.8421nm,c0=0.6094 nm;Z=4。
斜方雙錐晶類,D2h-mmm(3L23PC)。晶體少見,呈柱狀或針狀。主要單形:平行雙面b、c,斜方柱m、k、i,斜方雙錐p、r等。依(110)成雙晶,使晶體具假六方對稱外形。一般為致密粒狀、柱狀或針狀。
物理性質
白色,或被雜質染成灰、黃白、綠或褐色。玻璃光澤,斷口油脂光澤。解理中等,和不完全。硬度3.5~4。性脆。相對密度3.6~3.8。在陰極射線下發弱的淺藍光。
產狀與組合
為較少見的礦物。屬中、低溫熱液成因,呈脈狀產于石灰巖或泥灰巖中,與碳酸鋇礦、重晶石、方解石、天青石、螢石及硫化物共生。
鑒定特征
易溶于稀HCl并起泡。用吹管焰燒經HCl浸濕的樣品,火焰呈鮮 紅色。
工業應用
提取鍶的重要原料。碳酸鍶主要用于制造電視熒屏玻璃,可吸收γ射線;其次用于制造鍶鐵氧體。
- 相關百科
- 相關知識
- 相關專欄
- 碳酸鎳
- 碳酸鏑
- 碳酸飲料玻璃瓶
- 碳雕
- 碾米機磨粉機壓面機
- 磁傳感器及磁傳感器的制造方法
- 磁傾角
- 磁偏角
- 磁偏角度數
- 磁偏角零度線
- 磁共振成像原理
- 磁力偶矩
- 磁力共振
- 磁力分離滾筒
- 磁力勢能
- 磁力張力器
- 中國工程圖學學會成立工程與制造系統集成化分會
- 云計算技術在城市軌道交通運營指揮管理系統中的應用
- 多逆變器太陽能光伏并網發電系統的組群控制方法
- 智能建筑工程報警與電視監控系統前端設備的安裝施工
- 招遠電視臺制作播出系統數字化改造工程的設計與實踐
- 全熱回收地源熱泵空調機組的系統及工程方案設計
- 支持群體設計的工程數據庫管理系統的結構及實現
- 云計算對企業信息化系統建設和運營的影響分析和改進
- 智能建筑工程設計中的機電設備集成配置系統總體設計
- 智能電力監控管理系統在某飛機維修公司工程中的應用
- 智能建筑智能化工程名詞解釋-通信系統設備安裝工程
- 智能建筑虛擬儀器監控系統與控制網絡的接口技術
- 智能照明系統在高校教學樓建筑節能改造中的應用
- 醫用潔凈空調系統設計調試中易忽視的問題及設計優化
- 中關村太陽能集中集熱、分戶儲熱、分戶輔熱系統
- 多方式遠程控制門禁系統

