碳酸鈉晶體
碳酸鈉俗稱蘇打、石堿等,其晶體屬單斜晶系,又稱為碳酸鈉石。是重要的化工原料和食品添加劑。
碳酸鈉是白色粉末狀,分子式為Na2CO3,晶體稱碳酸鈉石。常溫下屬單斜晶系。440 ℃ 轉變β變體;500 ℃轉變為α變體,熔點為854℃。熔融狀態下晶格受到破壞,但仍保持短程的有序結構。碳酸鈉分子式為Na2CO3。與水反應生成,因反應溫度的不同會生成3種不同的結晶水合物,分別為一水合碳酸鈉(Na2CO3·H2O)、七水合碳酸鈉(Na2CO3·7H2O)以及十水合碳酸鈉(Na2CO3·10H2O)。
碳酸鈉的存在在自然界某些鹽湖或堿性土壤里常含有碳酸鈉。我國內蒙古自治區的某些鹽湖就出產天然堿(俗稱純堿)。
碳酸鈉晶體基本信息
| 中文名稱 | 碳酸鈉 | 化學式 | Na2CO3 |
|---|---|---|---|
| 熔????點 | 854℃ | 別????稱 | 蘇打、石堿 |
| 分子量 | 106 | 英文名 | soda |

碳酸鈉晶體侯氏制堿法
我國作為工業大國,工業發展是 尤為艱辛的.在制造純堿方面,成就顯著.我國著名化學家侯德榜被公認為是我國制堿業的先驅.上世紀二三十年代,當時較為先進的制堿技術都為歐美大國所壟斷.中國被迫進口高價的純堿.留學歸來的侯德榜看到這種情況暗暗立下決心,一定要打破歐美國家對制堿技術的壟斷,把中國的制堿業做大,做強.經過幾年的摸索,侯德榜和同事們攻克了一個又一個技術難題,創造性的發明了舉世聞名的"侯氏制堿法",為我國掌握成本低,質量高的制堿技術做出了重大貢獻.至今,他的名字還出現在中學教科書中,以此來記念這位偉大的科學家和愛國者.
碳酸鈉晶體造價信息
碳酸鈉俗稱石堿、蘇打、口堿。易溶于水,水解后呈顯堿性。 碳酸鈉從溶液里結晶析出時,晶體里結合著一定數目的水分子,這樣的水分子叫做結晶水。含有結晶水的碳酸鈉水合物叫做"水合碳酸鈉",與不含結晶水的碳酸鈉晶體有著本質的不同。水合碳酸鈉包括:Na2CO3·10H2O,Na2CO3·7H2O,Na2CO3·H2O等多種變體,常溫時放在干燥的空氣里,能逐漸失去結晶水而成為粉末,這種現象叫做風化。 碳酸鈉和碳酸鈣相似,跟鹽酸起反應都能生成二氧化碳氣體。 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 組成里含有CO3離子的鹽跟鹽酸起反應都能生成二氧化碳,利用這種反應既可以制取二氧化碳,又可以鑒別鹽類中是否含有CO3離子。
主要性質
碳酸鈉的商品名為純堿。視產品堆積密度的不同分為:超重質純堿、重質純堿、輕質純堿和超輕質純堿。碳酸鈉易溶于水,水溶液呈現堿性,可以與強酸、中強酸發生反應生產水與二氧化碳。
碳酸鈉是重要的基本化工原料之一,是進出口的大眾化工產品。碳酸鈉等在食品加工過程中經常使用的食品添加劑等有效成分構成,并已被科學實驗所證明,具有較高的安全性。
主要用途
碳酸鈉是化學工業的重要產品之一,它廣泛用在玻璃、造紙、紡織、洗滌劑等工業。
純堿工業史簡述
純堿的應用有著上千年的歷史,最早人類通過植物中提取或者通過堿性礦、堿水等大自然中獲取。后來,人類發明了呂布蘭發純堿制造技術(主要發生在固相之間的純堿生產技術),曾經風靡一時;十八世紀,比利時化學家索爾維在從事合成氨生產,用鹽水吸收氨時,無意間發現氨鹽水中通入二氧化碳后,發生了化學反應,得到了碳酸氫鈉結晶,碳酸氫鈉結晶通過煅燒分解可以獲取高純度的碳酸鈉(即純堿),從此至今,索爾維法純堿大型裝置工業化生產得到了迅速發展。
在我國,純堿工業鼻祖、著名的化學家侯德榜先生通過研究,攻克了索爾維法純堿技術秘密,并公開與世界,這又一次推動了世界純堿工業的發展。侯老先生研究發明了聯合制堿法,在生產純堿的同時副產氯化銨(化學氮肥)。并在天津永利堿廠成功投產。
純堿制造技術
呂布蘭法(已淘汰)、氨堿法(索爾維法)、聯堿法(侯氏制堿法、新旭法等)、天然堿加工法等。現在隨著工業技術的發展,在原有的純堿生產技術基礎上,衍生出了純堿與其他無機化工行業的優化結合的制堿新技術。
碳酸鈉晶體常見問題
-
基本介紹化學式Na2CO3 相對分子質量106 俗名塊堿、純堿、蘇打(Soda) 、堿面、口堿(歷史上,一般經張家口和古北口轉運全國,因此又有“口堿”之說。)、堿面(食用堿),無結晶水的工業名稱為輕質...
-
碳酸鈉的水溶液顯堿性,能使酚酞變紅。碳酸鈉的水溶液呈強堿性(pH=11.6)且有一定的腐蝕性,能與酸發生復分解反應,也能與一些鈣鹽、鋇鹽發生復分解反應。含有結晶水的碳酸鈉有3種:Na₂CO...
-
碳酸鈉只要保存好沒有有效期之說,跟食品不同,這是化學藥品。碳酸鈉只要不與空氣和水份接觸,單獨放置就不會變質。如果與空氣和水份接觸,視環境情況,有效期也不易定出。或許一天,或許仨月就變質了。中文別名:碳...
碳酸鈉晶體文獻

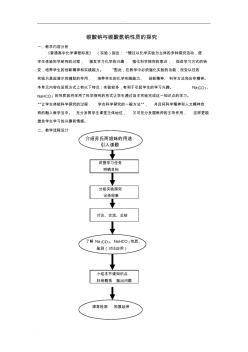 碳酸鈉與碳酸氫鈉性質的探究教學設計
碳酸鈉與碳酸氫鈉性質的探究教學設計
格式:pdf
大小:229KB
頁數: 9頁
評分: 4.6
. . 碳酸鈉與碳酸氫鈉性質的探究 一、教學內容分析 《普通高中化學課程標準》 (實驗)指出: “通過以化學實驗為主體的多種探究活動,使 學生體驗科學研究的過程, 激發學習化學的興趣, 強化科學探究的意識, 促進學習方式的轉 變,培養學生的創新精神和實踐能力。 ”因此,在教學中必須強化實驗的功能,改變以往的 實驗只是起演示和輔助的作用, 培養學生的化學實踐能力、 創新精神、 科學方法和合作精神。 本單元內容在呈現方式上有以下特點:實驗較多,有利于引起學生的學習興趣。 Na2CO3、 NaHCO 3 的性質我將采用了科學探究的形式讓學生通過自主實驗完成這一知識點的學習。 “讓學生體驗科學探究的過程, 學會科學探究的一般方法”, 并且將科學精神和人文精神自 然的融入教學當中。 充分發揮學生課堂主體地位, 又可充分發掘教師的主導作用, 這樣更能 激發學生學習的興趣和情感。 二、教學流程設計

 石灰-碳酸鈉軟化技術淺談
石灰-碳酸鈉軟化技術淺談
格式:pdf
大小:229KB
頁數: 4頁
評分: 4.4
青海云天化國際化肥有限公司 2019 年技術論文 ·1· 石灰 -碳酸鈉軟化技術淺談 張志軍 (青海云天化國際化肥有限公司氮肥產品部,青海湟中, 810000) 摘 要:軟化水作為水處理裝置的源頭,其軟化效果為后系統能否正常運行或最終出水指標的 控制發揮著重要作用。 石灰 -碳酸鈉軟化法作為國內經濟、 普遍的軟化處理工藝, 其控制和軟化效果 與單純的石灰軟化法相比有較大的差異,本文從工藝、原理、指標等方面作了進一步分析。 關鍵詞 : 原理 離子含量 硬度 溶度積 成本 1 概述 青海云天化化肥公司原水軟化裝置于 2016 年建成投產, 其主要工藝流程為: 園區 管網來水進入首先進入混凝劑投加池, 加聚 合硫酸鐵,通過攪拌機攪拌, 經快速混合后 進入石灰投加池, 然后進入絮凝池,絮凝池 中投加碳酸鈉和 PAM,不斷形成礬花。最后 進入沉淀池, 礬花下沉, 澄清水經斜管分離 后送下一工序。沉
為了儲存、運輸、使用的方便,工業上采用醇析出將其轉化成固態的過碳酸鈉晶體(化學式為:2Na2CO3·3H2O2),該晶體具有Na2CO3和H2O2的雙重性。
醇析出的產生工藝過程如下:在0~5℃時,往飽和Na2CO3溶液中,先加入H2O2和穩定劑(MgCl2和Na2SiO3),經充分反應后,再加入異丙醇,過濾,分液,即得過碳酸鈉晶體。 經過處理可得到粒粒氧,即固粒氧,用于在魚池中立體增氧,凈化水質。
其合成工藝條件溫和、設備簡單、操作方便。
過碳酸鈉能用于生產H2O2,過氧化氫(H2O2)俗名雙氧水,
常溫下是一種無色的液體,它難電離,易分解。作為一種經典化工產品,工業上早在一百多年前便開始生產。隨著社會需求的增長,尤其是生態環境保護的需要,過氧化氫近年來更受人們的青睞,并被稱為"綠色氧化劑"。為了儲存、運輸、使用的方便,工業上采用醇析出將其轉化成固態的過碳酸鈉晶體(化學式為:2Na2CO3·3H2O2),該晶體具有Na2CO3和H2O2的雙重性。醇析出的產生工藝過程如下:在0~5℃時,往飽和Na2CO3溶液中,先加入H2O2和穩定劑(MgCl2和Na2SiO3),經充分反應后,再加入異丙醇,過濾,分液,即得過碳酸鈉晶體。 經過處理可得到粒粒氧,即固粒氧,用于在魚池中立體增氧,凈化水質。洗滌劑的多功能化,即在洗滌去污的同時,兼有漂白、殺菌、消毒等作用,已成為洗滌劑的發展趨勢,國外很多洗滌劑都加有起漂白作用的組分,國內也逐漸向這方面發展。由于過碳酸鈉無味、無毒,冷水中易于溶解,去污力強,溶于水后能放出氧而起到漂白殺菌等多種功效,符合現代洗滌劑發展潮流。傳統粉狀洗滌劑多用過硼酸鈉,但過硼酸鈉存在溶解速度慢、價格較貴以及硼元素對農作物有影響等缺點。而過碳酸鈉比過硼酸鈉成本低,溶解性好,適宜寒冷地區和冬天使用,又不會對農作物產生危害,因此過碳酸鈉在洗滌劑生產中應用日益增多,目前,過碳酸鈉已廣泛用作家用和工業用洗滌、漂白、殺菌劑,用于合成纖維、動物纖維、合成樹脂纖維、紙漿脂等生產領域,漂白效果好,不損傷面料,不泛黃。
- 相關百科
- 相關知識
- 相關專欄
- 自動旋光儀
- 四通PS-2000S/2H
- 純堿制造技術
- 羅蘭西尼
- 臨沂市蘭山區建銳鋸片行
- 層間短路
- 四通SD-500S
- 純堿工學
- 旋光儀
- 切角機
- 高強度精軋螺紋鋼
- 四通PS-3000
- 濕式氣體流量計
- 四通PS-6000/2H
- 四通SD-1000
- 磁化凈水器
- 中國電科閃爍及激光晶體項目在龍巖稀土工業園區開工
- 復合材料的蛋白石結構光子晶體制備及表征
- LED藍寶石晶體項目可行性報告
- 場板抑制GaN高電子遷移率晶體管電流崩塌的機理
- 傅里葉紅外光譜測量人造石英晶體紅外質量指標
- 帶有環形諧振器的1×2光子晶體功率分配器傳輸性能
- 摻鍺芯光子晶體光纖和普通單模光纖的低損耗熔接
- 中低合金鋼板條馬氏體和下貝氏體的晶體學相似性
- 單層膠體晶體及反蛋白質納米陣列結構的制備
- 地面用晶體硅光伏組件最大功率測量不確定度分析
- 單電子晶體管的蒙特卡羅模擬及宏觀建模英文
- 柚子型光子晶體光纖布拉格光柵理論及實驗
- 開關穩壓IC輸出電流增大雙極晶體管
- 光子晶體光纖壓力傳感器輸出信號監測技術
- 環形諧振器的T型光子晶體功率分配器特性
- 100MW晶體硅太陽能光伏發電站建設項目
