增烴水煤氣水煤氣
亦稱蘭焰水煤氣。是一種比較清潔的低級(jí)燃料氣,主要用于工業(yè)中對(duì)材料加熱以及用作爐子的燃料。水煤氣是使過熱蒸汽通過紅熱的焦炭床而產(chǎn)生出來的。蒸汽部分地使碳氧化形成一氧化碳,而它本身則還原為氫氣。水煤氣的主要成分是一氧化碳(40至45%)和氫(45至51%),其比例視反應(yīng)條件而定。水煤氣還含一些二氧化碳、怎和微量的甲烷。一氧化碳和氫都是可燃的,但此混合氣的熱值不很高,約為350英熱單位/英尺(13.0兆焦耳/米)。
蒸汽與焦炭之間的反應(yīng)要吸熱,使焦炭床的溫度急劇下降。因此,焦炭床要用吹氣再加熱。這樣就使過程成為斷續(xù)的一一焦炭再加熱吹氣的一分鐘,再送蒸汽三分鐘。
吹氣階段產(chǎn)生的水煤氣常常經(jīng)煙道排出而浪廢掉。但是,如果焦炭床足夠厚,吸氣階段就可產(chǎn)生出叫作發(fā)生爐煤氣的一氧化碳和氮的混合氣。由于一氧化碳也是可燃的,可以與水煤氣相混合,這樣主要由一氧化碳、氫和氮組成的混合氣叫作半水煤氣。
增烴水煤氣造價(jià)信息
使蒸汽通過熱焦炭而制成的水煤氣,為提高水煤氣濃度還使粗柴油同時(shí)通過焦炭。最終產(chǎn)品增烴水煤氣的熱值約500英熱單位/立方英尺(18.7兆焦耳/立方米)。增烴水煤氣由美國早在上世紀(jì)發(fā)明的方法生產(chǎn),而且是用石油產(chǎn)品生產(chǎn)煤氣的第一種應(yīng)用場(chǎng)合。
生產(chǎn)水煤氣一般用焦炭作燃料,因?yàn)榻固康奶己亢颓鍧嵍榷己芨摺R灿杏脽o煙煤、煙煤以及煤和焦炭的混合物的,而且較為成功,但是整個(gè)操作效率要有些降低。
水煤氣燃燒時(shí)帶有明亮的藍(lán)火焰,所以稱為“藍(lán)水煤氣”。水煤氣用于許多化學(xué)工程,可以為合成工藝的基本燃?xì)猓遣灰擞米骷彝ト剂希怯脽峤獾娜剂嫌驮鰺N,制得所謂的增烴水煤氣。
焦炭制得的水煤氣然燒時(shí)不帶光焰,而增烴水煤氣燃燒時(shí)具有很強(qiáng)的光焰,不過,這兩種水煤氣的燃燒速度超過其它任何廣泛使用的燃?xì)猓辉鰺N水煤氣的燃燒速度實(shí)際上與焦?fàn)t煤氣相當(dāng)。水煤氣的比重比天然氣的稍小一點(diǎn),但是比焦?fàn)t煤氣要大;增烴水氣比重比天然氣大,但是比發(fā)生爐煤氣要小。藍(lán)水煤氣和增烴水煤氣兩者的理論火焰溫度很,分別約為2020°C和2050°C,超過通常使用的所有其它工業(yè)燃?xì)狻_@兩種水煤氣都具有相當(dāng)寬的爆炸范圍。
增烴水煤氣水煤氣常見問題
-
水煤氣其實(shí)就是水蒸氣和灼熱的焦炭反應(yīng)。水蒸氣和灼熱的焦炭在高溫的條件下反應(yīng)生成氫氣和:H2O+C=高溫=H2+CO(反應(yīng)物的水是以水蒸氣氣態(tài)的形式存在,所以生成物的氣體不需要標(biāo)氣體符號(hào))。然后生成的氫...
-
水煤氣行業(yè)的“工業(yè)革命” ——洛陽豫燃”兩步法水煤氣制造工藝” 撰稿 張金輝 肖繼平 指導(dǎo) 陶予敏 邁入二十一世紀(jì),人類不得不承認(rèn),伴隨著新科技,新文明的到來.能源危機(jī)的紅燈頻頻亮起。石油、煤炭、天然...
-
套鋼管敷設(shè)子目。
增烴水煤氣水煤氣文獻(xiàn)

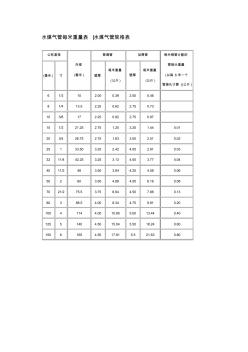 水煤氣鋼管表
水煤氣鋼管表
格式:pdf
大小:26KB
頁數(shù): 1頁
評(píng)分: 4.5
水煤氣管每米重量表 |水煤氣管規(guī)格表 公稱直徑 外徑 (毫米 ) 普通管 加厚管 每米鋼管分配的 管接頭重量 (以每 6米一個(gè) 管接頭計(jì)算 )(公斤 ) (毫米 ) 寸 壁厚 每米重量 (公斤 ) 壁厚 每米重量 (公斤 ) 6 1/3 10 2.00 0.39 2.50 0.46 8 1/4 13.5 2.25 0.62 2.75 0.73 10 3/8 17 2.25 0.82 2.75 0.97 15 1/2 21.25 2.75 1.25 3.25 1.44 0.01 20 3/4 26.75 2.75 1.63 3.50 2.01 0.02 25 1 33.50 3.25 2.42 4.00 2.91 0.03 32 11/4 42.25 3.25 3.13 4.00 3.77 0.04 40 11/2 48 3.50 3.84 4.25 4.58 0.06

 焦?fàn)t煤氣配半水煤氣生產(chǎn)合成氨擴(kuò)能改造
焦?fàn)t煤氣配半水煤氣生產(chǎn)合成氨擴(kuò)能改造
格式:pdf
大小:26KB
頁數(shù): 4頁
評(píng)分: 4.4
分析了山西豐喜華瑞煤化工公司焦?fàn)t煤氣配半水煤氣生產(chǎn)合成氨18-30項(xiàng)目生產(chǎn)工藝流程,結(jié)合周邊焦化廠富余焦?fàn)t煤氣的實(shí)際供應(yīng)情況,對(duì)原工藝流程進(jìn)行優(yōu)化,改造方案為:增加變壓吸附提氫工序、強(qiáng)化甲烷轉(zhuǎn)化工藝條件、增加部分設(shè)備等。通過改造,可使合成氨生產(chǎn)能力由18萬t/a提高到24萬t/a、尿素生產(chǎn)能力由30萬t/a提高到40萬t/a,取得較好的經(jīng)濟(jì)效益和社會(huì)效益。
炔烴是一類有機(jī)化合物,屬于不飽和烴。其官能團(tuán)為碳碳三鍵(-C≡C-)。直鏈單炔烴的通式CnH2n-2,其中n為≥2的正整數(shù)。簡(jiǎn)單的炔烴化合物有乙炔(C2H2)、丙炔(C3H4)等。炔烴原來也被叫做電石氣,電石氣通常也被用來特指炔烴中最簡(jiǎn)單的乙炔。
“炔”字是新造字,左邊的火取自“碳”字,表示可以燃燒;右邊的夬取自“缺”字,表示氫原子數(shù)和化合價(jià)比烯烴更加缺少,意味著炔是烷(完整)和烯(稀少)的不飽和衍生物。
簡(jiǎn)單的炔烴的熔點(diǎn)、沸點(diǎn),密度均比具有相同碳原子數(shù)的烷烴或烯烴高一些。不易溶于水,易溶于乙醚、苯、四氯化碳等有機(jī)溶劑中。炔烴可以和鹵素、氫、鹵化氫、水發(fā)生加成反應(yīng),也可發(fā)生聚合反應(yīng)。 因?yàn)槿苍谌紵龝r(shí)放出大量的熱,炔又常被用來做焊接時(shí)的原料。
近幾年來,正在開發(fā)高溫氣冷堆的技術(shù),用氦為熱載體將核反應(yīng)熱轉(zhuǎn)送至氣化爐作為熱源,以生產(chǎn)水煤氣。
炔烴的一般制備是通過鄰二鹵化烷烴的脫鹵化氫作用,也可以通過金屬炔化合物與一級(jí)鹵化烷反應(yīng)制得。在Fritsch-Buttenberg-Wiechell重排中,炔烴又溴化乙烯基起始制得。
炔烴也可以由醛通過Corey-Fuchs反應(yīng)制得,亦可以通過Seyferth-Gilbert同素化制得。
乙炔制作用煤或石油作原料,是生產(chǎn)乙炔的兩種主要途徑。隨著天然氣化學(xué)工業(yè)的發(fā)展,天然氣即將成為乙炔的主要來源。
炔烴電弧法
甲烷在1500℃電弧中經(jīng)極短時(shí)間(0.1~0.01s)加熱,裂解成乙炔,即:
2CH4→C2H2 3H2,ΔH=397.4KJ/mol
由于乙炔在高溫很快分解成碳,故反應(yīng)氣須用水很快地冷卻,乙炔產(chǎn)率約15%,改用氣流冷卻反應(yīng)氣,可提高乙炔產(chǎn)率達(dá)25%~30%。裂解氣中還含有乙烯、氫和碳?jí)m。這個(gè)方法的總特點(diǎn)是原料非常便宜,在天然氣豐富的地區(qū)采用這個(gè)方法是比較經(jīng)濟(jì)的。石腦油也可用此方法生產(chǎn)乙炔。
炔烴電石法
用焦炭和氧化鈣經(jīng)電弧加熱至2200℃,制成碳化鈣(CaC2),它再與水反應(yīng),生成乙炔和氫氧化鈣:
CaO 3C<—2200℃—>CaC2 CO,ΔH=460kJ/mol
CaC2 2H2O——>C2H2 Ca(OH)2
此法成本較高,除少數(shù)國家外,均不用此法。
炔烴等離子法
用石油和極熱的氫氣一起熱裂制備乙炔,即把氫氣在3500~4000℃的電弧中加熱,然后部分等離子化的等離子體氫(正負(fù)離子相等)于電弧加熱器出口的分離反應(yīng)室中與氣體的或氣化了的石油氣反應(yīng),生成的產(chǎn)物有:乙炔、乙烯(二者的總產(chǎn)率在70%以上)以及甲烷和氫氣。
乙炔過去是非常重要的有機(jī)合成原料,由于乙炔的生產(chǎn)成本相當(dāng)高,以乙炔為原料生產(chǎn)化學(xué)品的路線逐漸被以其他化合物(特別是乙烯、丙烯)為原料的路線所取代。
純的乙炔是帶有乙醚氣味的氣體,具有麻醉作用,燃燒時(shí)火焰明亮,可用以照明。工業(yè)乙炔不好聞氣味是由于含有硫化氫、磷化氫、以及有機(jī)磷、硫化合物等雜質(zhì)引起的。與乙烯、乙烷不同,乙炔在水中具有一定的溶解度,但易溶于丙酮。液化乙炔經(jīng)碰撞、加熱可發(fā)生劇烈爆炸,乙炔與空氣混合、當(dāng)它的含量達(dá)到3~70%時(shí),會(huì)劇烈爆炸。商業(yè)上為安全地處理乙炔,把它裝入鋼瓶中,瓶?jī)?nèi)裝有多孔材料,如硅藻土、浮石或木炭,再裝入丙酮。丙酮在常壓下,約可溶解相當(dāng)于它體積25倍的乙炔,而在1.2MPa下可溶解相當(dāng)其體積300倍的乙炔。乙炔和氧氣混合燃燒,可產(chǎn)生2800℃的高溫,用以焊接或切割鋼鐵及其他金屬。
- 相關(guān)百科
- 相關(guān)知識(shí)
- 相關(guān)專欄
- 增量計(jì)算法
- 增長(zhǎng)型永續(xù)年金
- 墨溝石灰?guī)r
- 墨輪打碼機(jī)
- 墨輥
- 壁畫取暖器
- 壁虎(英國)有限公司
- 壁面熱流
- 壕豬刺
- 壤塘縣發(fā)展和改革委員會(huì)
- 壤塘縣建筑安裝裝飾工程公司
- 士興國際集團(tuán)
- 聲光材料
- 聲卡芯片廠家
- 聲威W001
- 聲子晶體型壓電換能器的設(shè)計(jì)原理和實(shí)驗(yàn)研究
- 桃山水庫二期工程增容與興凱湖調(diào)水的關(guān)系
- 增設(shè)鋼牛腿在連續(xù)獨(dú)柱墩橋梁抗傾覆加固設(shè)計(jì)中的應(yīng)用
- 增效劑在水工高性能混凝土中增效機(jī)理及其應(yīng)用
- 云南綠水河二級(jí)電站4號(hào)水輪機(jī)增容技術(shù)改造效果分析
- 增城區(qū)農(nóng)村小型工程建設(shè)項(xiàng)目施工企業(yè)庫房屋建筑工程
- 增粘劑PN759在橡膠與鋼絲簾線粘合中的應(yīng)用
- 增韌雙馬來酰亞胺樹脂及其玻璃布層壓板的制備與性能
- 中國熱水管道增壓泵價(jià)格行業(yè)十大立式自吸泵品牌首選
- 增強(qiáng)水泥(GRC)聚苯復(fù)合板外墻保溫施工工藝標(biāo)準(zhǔn)
- 增強(qiáng)整體效益促進(jìn)持續(xù)發(fā)展:談建筑熱環(huán)境改善與節(jié)能
- 增大截面與CFRP復(fù)合加固素混凝土短圓柱試驗(yàn)
- 增設(shè)Ⅱ型電動(dòng)輪汽車主發(fā)電機(jī)磁場(chǎng)電流監(jiān)測(cè)信號(hào)的構(gòu)思
- 增建二線鐵路線間距偏小地段石方爆破施工工藝
- 增強(qiáng)水文與水資源工程專業(yè)本科生畢業(yè)實(shí)習(xí)效果的思考
- 營(yíng)改增背景下建筑企業(yè)財(cái)務(wù)管理所受影響及應(yīng)對(duì)策略
- 應(yīng)用新型高性能水輪機(jī)轉(zhuǎn)輪對(duì)老電站水電機(jī)組增容改造